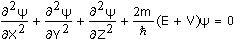Alkana yang paling sederhana adalah metana. Alakana merupakan hidrokarbon yang terdiri atas ikatan tunggal, alkana juga bisa disebut paraffin yang berarti sesuatu yang sukar bereaksi. Rumus umum alkana adalah C2H2n+2, dengan n ialah banyak atom karbon. Penggantian atom H oleh atom C yang lain akan menghasilkan suatu deret homolog (sepancaran), yaitu suatu seri susunan hidrokarbon yang setiap anggota berbeda sebanyak –CH2– dari anggota berikutnya.
Sistem Nomenklatur
Setiap molekul dalam penamaannya terbagi atas tiga bagian, yakni :
- Parent (rantai induk)
- Prefix (cabang)
- Suffix (gugus fungsi)
Sistem nomenklatur alkana ditulis dengan mengikuti system UIPAC (the International Unoin of Pure and Applied Chemistry). Berikut aturan IUPAC untuk penamaan alkana, secara ringkas :
- Cari rantai karbon lurus terpanjang. Ini menghasilkan nama hidrokarbon induk (parent). Contohnya :
C—C C—C
C—C—C—C bukan C—C—C—C
- Nomori rantai terpanjang mulai dari ujung yang terdekat dengan cabang pertama. Contohnya :
1 2 3 4 5 6 6 5 4 3 2 1
C—C—C—C—C—C bukan C—C—C—C—C—C
C C
Jika ada dua rantai lurus terpanjang yang sama, pilihlah rantai yang palig banyak cabangnya. Contohnya :
| 3 4 5 6 |
| 1 2 3 4 5 6 |
C C
C—C—C—C—C—C bukan C—C—C—C—C—C
| 1 2 |
C—C C—C
- Tulislah namanya sebagai satu kata, letakan subtituen dalam urutan abjad dan gunakan tanda baca dengan benar.
| RUMUS MOLEKUL | NAMA |
| CH4 | Metana |
| C2H6 | Etana |
| C3H8 | Propana |
| C4H10 | Butana |
| C5H12 | Pentana |
| C6H14 | Heksana |
| C7H16 | Heptana |
| C8H18 | Oktana |
| C9H20 | Nonana |
| C10H22 | Dekana |
| C11H24 | Undekana |
| C12H24 | Dodekana |
| C13H26 | Tridekana |
| C14H30 | Tetradekana |
| C15H32 | Pentadekana |
| C16H34 | Heksadekana |
| C17H36 | Heptadekana |
| C18H38 | Oktadekana |
| C19H40 | Nonadekana |
| C20H42 | Eiksona |
Isomer Struktural
Isomer adalah senyawa-senyawa yang mempunyai rumus molekul sama. Keisomeran dapat terjadi karena perbedaan stuktur, perbedaan konfigurasi, dan sifatnya. Struktur menggambarkan bagaimana atom-atom saling berkaitan dalam satu molekul, yaitu menggambarkan apa mengikat apa, sedangkan konfigurasi menggambarkan susunan runag atom-atom dalam satu molekul.
Isomer Struktural merupakan isomer yang mempunyai rumus molekul yang sama, namun memiliki bentuk yang berbeda dan pastikan bahwa menunjukkan sifat kimia dan sifat fisika yang berbeda pula. Isomer struktur terdiri atas :
- Isomer Rantai
Isomer ini muncul karena percabangan rantai karbon. Isomer rantai merupakan isomer yang disebabkan oleh perbedaan susunan rantai karbon. Sebagai contoh C4H10 yakni antara n-butana dengan isobutana
C
C—C—C—C dengan C—C—C
Selain perbedaan stuktur rantainya yang terliht jelas, isomer ini dibedakan dengan salah satu sifat fsikanya yakni n-butana memiliki titik didik -0,4°C sedangkan isobutana memiliki titik didih -10°C , dari sifat kimianya n-butana lebih stabil jika dibandingkan dengan isobutana karena isobutana memiliki halangan sterik yang tinggi sehingga memiliki energi yang tinggi pula.
- Isomer Posisi
Isomer ini muncul jika cabang gugus fungsi yang berpindah-pindah tempat. Dalam isomer posisi, isomer ini memiliki kerangka karbon induk yang tetap, namun kelompok-kelompok penting yang berpindah-pindah pada kerangka itu. Isomer yang disebabkan oleh perbedaan letak gugus fungsi. Sebagai contoh 1-propanol dengan 2-propanol.
C—C—C—OH dengan C—C—C
OH
- Isomer Fungsional
Isomer ini muncul jika memiliki gugus fungsional yang berbeda. Keisomeran fungsional terjadi antara senyawa dengan rumus molekul sama, tetapi berbeda gugus fungsinya. Sebagai contoh dimetil eter dengan etanol
CH3—O—CH3 dengan CH3—CH2—OH
Ditinjau dari sifat fisisnya etanol memiliki titik didih yang lebih tinggi jika dibandingkan dengan dimetil eter. Jika ditinjau dari sifat kimianya etanol lebih reaktif dibandingkan dengan dimetil eter.
Penyebab sudut ikatan H—C—C lebih besar dibandingkan sudut ikatan H—C—H.
Bentuk molekul menggambarkan kedudukan atom-atom di dalam suatu molekul, yaitu kedudukan atom-atom dalam ruang tiga dimensi dan besarnya sudut-sudut ikatan yang dibentuk dalam suatu molekul, serta ikatan yang terjadi pada molekul tersebut yang dibentuk oleh pasangan-pasangan elektron. Teori Domain Elekton menjelaskan susunan elektron dalam suatu atom yang berikatan. Posisi elektron ini akan mempengaruhi bentuk geometri molekulnya dan bentuk geometri ini akan dijelaskan melalui teori VSEPR. Menurut teori ini, meskipun kedudukan pasangan elektron dapat tersebar diantara atom-atom tersebut, tetapi secara umum terdapat pola dasar kedudukan pasangan-pasangan elektron akibat adanya gaya tolak-menolak yang terjadi antara pasangan elektron.
Bentuk molekul H—C—C adalah pola linear yakni atom-atomnya tertata dalam satu garis lurus. Sudut yang dibentuk oleh dua ikatan ke arah atom pusat akan saling membentuk sudut 180°. Sedangkan Bentuk molekul H—C—H adalah pola segitiga planar yakni atom-atom dalam molekul berbentuk segitiga tertata dalam bidang datar,tiga aton akan berada pada titik sudut segitiga sama sisi dan dipusat segitiga terdapat atom pusat. Sudut ikatan antara atom yang mengelilingi atom pusat membentuk sudut 120°. Hal inilah yang menyebabkan sudut ikatan H—C—C lebih besar dibandingkan sudut ikatan H—C—H.